Tésamoréline en recherche 2026 : mécanisme GHRH, données NAFLD Lancet 2019, et l’arrivée d’EGRIFTA WR F8
La tésamoréline (TH9507) est l’unique GHRH-analogue à avoir franchi le couloir réglementaire jusqu’à l’AMM clinique, depuis 2010 sous Egrifta® pour la lipodystrophie associée au VIH. En mars 2025, la FDA a approuvé EGRIFTA WR, formulation F8 huit fois plus concentrée que l’originale, qui change la pratique. Mais l’intérêt de recherche moderne sort largement du cadre HIV : NAFLD, fibrose hépatique, cognition. Voilà ce que la littérature peer-reviewed dit vraiment sur cette molécule.

Tésamoréline 2026 : la fiche technique en un tableau
| Caractéristique | Donnée |
|---|---|
| Classe pharmacologique | GHRH-analogue stabilisé |
| Séquence | 44 acides aminés, modification trans-3-hexenoique N-terminale |
| CAS | 218949-48-5 |
| Masse moléculaire | ~5 196 Da |
| Demi-vie plasma | 26 à 60 minutes |
| Récepteur cible | GHRH-R (Gαs / cAMP / PKA) |
| Statut FDA | Egrifta® 2010, Egrifta SV F4 2019, EGRIFTA WR F8 mars 2025 |
| Statut EMA | Pas d’AMM centralisée, procédures nationales |
| Statut WADA | Liste S2 (hormones peptidiques, facteurs de croissance) |
| Prix recherche FP | 29 € (5 mg) à 49 € (10 mg), pureté HPLC ≥98 % |
La tésamoréline reste la référence GHRH-analogue avec validation clinique humaine, ce qui en fait un composé d’étude particulièrement intéressant pour les laboratoires qui veulent comparer un GHRH-analogue à pharmacocinétique connue versus le CJC-1295 (DAC ou no DAC) ou le sermorelin natif.
Mécanisme moléculaire : ce que la modification trans-3-hexenoique change vraiment
Le GHRH humain natif fait 44 acides aminés et a une demi-vie plasmatique d’environ 7 minutes. Son talon d’Achille : la dipeptidyl peptidase-IV (DPP-IV) clive le peptide après les résidus 2-3 et désactive la molécule en quelques minutes. C’est ce qui explique pourquoi le GHRH endogène fonctionne par micro-pulses tonique-pulsatiles, pas par flux soutenu.
La tésamoréline, c’est le GHRH humain 1-44 avec une modification chimique en N-terminal : un groupement trans-3-hexenoique greffé sur le résidu Tyr¹. Cette acylation bloque le site de reconnaissance par la DPP-IV. Conséquence directe : la demi-vie passe de 7 minutes à 26-60 minutes selon les études. Le peptide n’est plus une cible enzymatique, il a le temps de se fixer sur le récepteur GHRH-R des cellules somatotropes hypophysaires et de déclencher la libération de GH.
Cascade Gαs/cAMP préservée
Une fois fixée sur le GHRH-R, la tésamoréline active la même cascade que le GHRH natif : protéine Gαs → adénylate cyclase → cAMP → PKA → phosphorylation de CREB → transcription du gène GH. Pas de raccourci, pas de mécanisme parallèle, juste une activation prolongée du circuit physiologique habituel. C’est ce qui distingue le tésamoréline d’une administration directe de somatropine recombinante : on stimule la sécrétion endogène, on n’apporte pas l’hormone exogène.
Pulsatilité conservée et feedback intact
Donnée importante que les comparatifs concurrents oublient souvent : la tésamoréline préserve le pattern pulsatile naturel de la GH. Le rétrocontrôle hypothalamus → hypophyse → IGF-1 → somatostatine reste fonctionnel. Si le système accumule trop de signal, la somatostatine vient inhiber la libération suivante. Cette caractéristique différencie nettement la tésamoréline d’une perfusion continue de GH où le feedback est pratiquement aboli.
Falutz 2007 (NEJM) : l’essai pivot qui a justifié l’AMM clinique
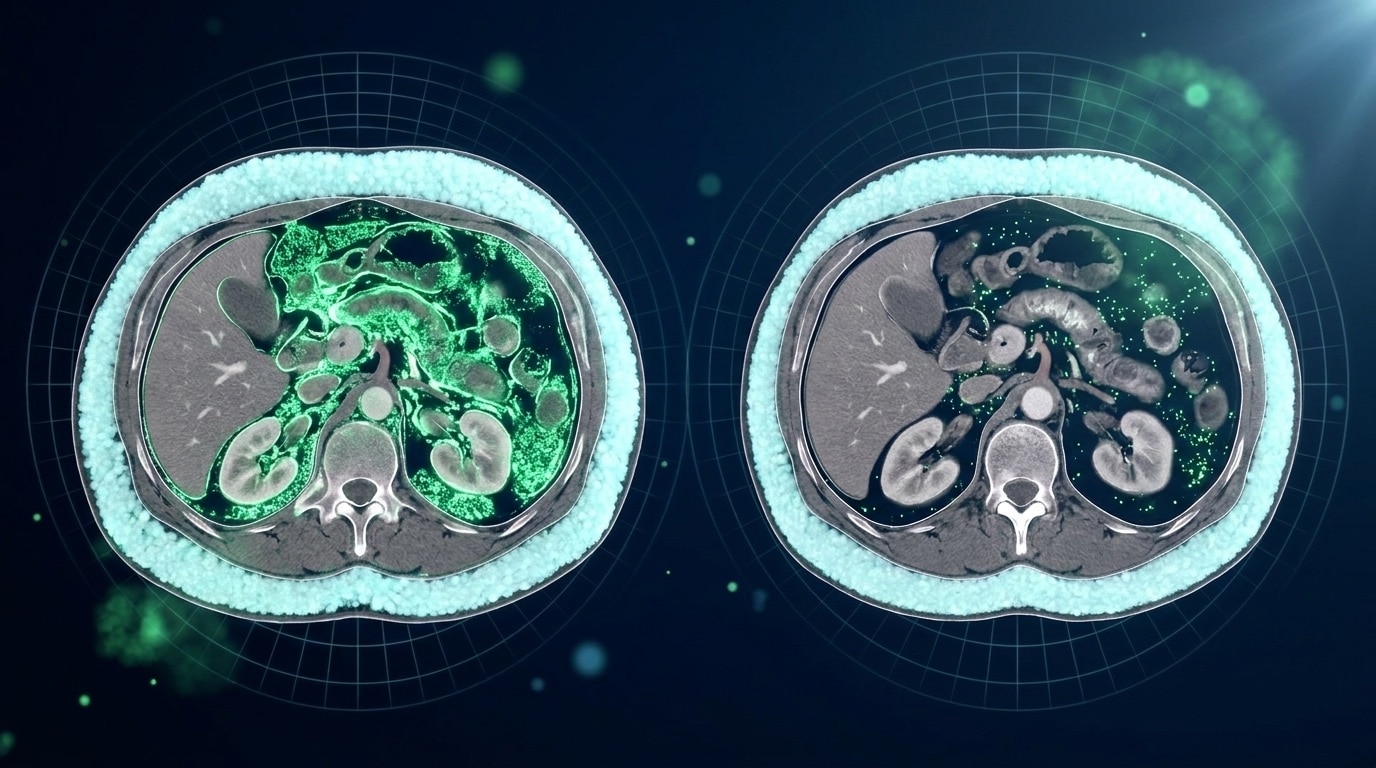
L’essai phase 3 publié dans le New England Journal of Medicine en 2007 par Julian Falutz et collègues reste la référence pour la pharmacologie clinique humaine de la tésamoréline. Voici les données précises, pas la version simplifiée des forums.
Design
Étude randomisée en double-aveugle contre placebo sur 412 patients VIH adultes avec lipodystrophie centrale (accumulation excessive de graisse viscérale liée aux antirétroviraux). 26 semaines de traitement, 2 mg/jour en sous-cutané dans la zone abdominale. Imagerie scanner abdominale L4-L5 pour mesurer la graisse viscérale (VAT, visceral adipose tissue) à T0 et T26.
Résultats principaux
- VAT viscéral : -15,2 % chez le groupe tésamoréline versus +5,0 % chez le placebo (p < 0,001).
- VAT sous-cutané : pas de modification significative. La molécule cible spécifiquement le compartiment viscéral.
- IGF-1 sérique : +81,0 % chez tésamoréline versus -5,0 % placebo (p < 0,001).
- Triglycérides : baisse significative, profil lipidique amélioré.
- Tolérance : bien toléré, événements indésirables principalement injection-site (érythème, douleur locale).
Étude d’extension à 52 semaines
L’essai TH9507-CTR-1011 a poursuivi le suivi sur 52 semaines avec maintien du traitement. Réduction VAT prolongée jusqu’à -18 % à 1 an. Critique : interruption du traitement entraîne un retour progressif vers les valeurs baseline en 6-9 mois, ce qui démontre que l’effet n’est pas de “rééducation métabolique” mais bien d’une stimulation pharmacologique active.
Stanley 2019 (Lancet HIV) : -37 % de graisse hépatique dans la NAFLD associée au VIH
L’extension la plus significative de la recherche tésamoréline depuis 2015 vise la stéatose hépatique non alcoolique (NAFLD, désormais souvent appelée MASLD/MASH). La graisse hépatique est mesurée par spectroscopie en résonance magnétique du proton (¹H-MRS), méthode beaucoup plus précise que les marqueurs sériques.
Design (Stanley et al., Lancet HIV 2019)
Étude randomisée en double-aveugle multicentrique. 61 patients VIH avec hepatic fat fraction (HFF) ≥ 5 % par ¹H-MRS. Randomisation 1:1, tésamoréline 2 mg/jour ou placebo pendant 12 mois, suivi d’une phase open-label 6 mois où tous les participants reçoivent la tésamoréline.
Résultats
- Réduction absolue HFF : -4,1 % (IC 95 % -7,6 à -0,7, p = 0,02) chez le groupe tésamoréline.
- Réduction relative HFF : -37 % (IC 95 % -67 à -7, p = 0,02). C’est-à-dire qu’un foie démarrant à 10 % de graisse passe à 6,3 % en moyenne.
- Fibrose hépatique : prévention de la progression à 12 mois, mesurée par enhanced liver fibrosis (ELF) score et FibroScan.
- Mécanisme inféré : la stimulation IGF-1 chronique modifie le profil lipogénique hépatique. Étude de transcriptomique 2020 (Fourman et al., JCI Insight) a confirmé une signature transcriptomique compatible avec une réduction de la lipogenèse de novo.
EGRIFTA WR (mars 2025) : la formulation F8 qui change la pratique clinique
Le 25 mars 2025, la FDA a approuvé le supplemental Biologics License Application (sBLA) de Theratechnologies pour EGRIFTA WR™, formulation F8 de la tésamoréline. C’est la troisième formulation depuis 2010 et celle qui change concrètement la vie des patients sous traitement.
Différences techniques entre F1, F4 (SV) et F8 (WR)
| Formulation | Année AMM | Concentration | Reconstitution | Dose |
|---|---|---|---|---|
| Egrifta F1 | 2010 | Référence baseline | Quotidienne | 2 mg/j (volume élevé) |
| Egrifta SV F4 | 2019 | 4× F1 | Quotidienne | 2 mg/j (volume divisé /4) |
| EGRIFTA WR F8 | mars 2025 | 8× F1, 2× F4 | Hebdomadaire | 1,28 mg/j (0,16 mL) |
Détails F8
EGRIFTA WR est conditionné en 4 flacons single-patient-use de 11,6 mg de tésamoréline. Chaque flacon couvre 7 doses, donc un flacon = 1 semaine de traitement. La reconstitution se fait une fois par semaine, et la solution se conserve 7 jours à +2-8 °C, ce qui simplifie nettement la logistique.
Bioequivalence avec la F1 originale confirmée par études pharmacocinétiques. Profil PK identique (Cmax, Tmax, AUC), donc l’efficacité clinique attendue est identique à celle des essais Falutz 2007 et Stanley 2019. Indication AMM inchangée : adultes VIH avec lipodystrophie et excès de graisse abdominale viscérale documenté.
Cognition et tésamoréline : ce que les essais 2024-2025 montrent (et ce qu’ils ne montrent pas)

L’idée que la stimulation chronique de l’axe GH/IGF-1 puisse améliorer la fonction cognitive vient d’une observation simple : les adultes avec déficit GH démontré présentent souvent un déclin cognitif modéré, et le traitement par GH ou GHRH peut le compenser partiellement. Plusieurs essais ont testé cette hypothèse avec la tésamoréline.
Trial Baker 2012 (Alzheimer’s & Dementia)
Un essai contrôlé randomisé chez des adultes âgés sains et patients avec mild cognitive impairment a rapporté en 2012 une amélioration de la fonction exécutive et de la mémoire de travail après tésamoréline 1 mg/jour pendant 20 semaines. Effet de taille modeste mais statistiquement significatif (Baker et al., 2012).
Phase II HIV NCT02572323 : résultat plus nuancé
L’essai NCT02572323 conduit à UCSD et USC a recruté 140 sujets VIH+ âgés 40-70 ans avec obésité abdominale et troubles neurocognitifs HIV-associés réversibles. Randomisation 3:2 tésamoréline:placebo sur 9 mois.
Résultats publiés en janvier 2025 (PMID 39813152) : l’effet sur le tour de taille est confirmé (réduction significative), mais l’effet sur la fonction neurocognitive globale (mesurée par global deficit score) n’a pas significativement différé entre les groupes à 6 mois. Pas de bénéfice cognitif clair sur cette durée de traitement chez cette population.
Tésamoréline recherche : tarifs et combos chez French Peptides 2026
| Produit | Format | Prix | Pureté HPLC |
|---|---|---|---|
| Tésamoréline | 5 mg / 10 mg | 29 € / 49 € | ≥98 % |
| Combo Tésamoréline + Ipamorelin | 10 mg pré-formulé | 89 € | ≥98 % |
Reconstitution standard : 5 mg de lyophilisat dans 2 mL d’eau bactériostatique donne 2,5 mg/mL. Sur seringue insuline U-100, 1 unité = 25 µg de tésamoréline. Un palier de 1 mg correspond à 40 unités, un palier 2 mg à 80 unités. Ces conversions sont identiques à celles documentées pour le CJC-1295, donc cohérence dans les protocoles labo qui comparent les deux GHRH-analogues.
Pour le panorama prix complet face à la somatropine pharmacie et aux autres GHRH-analogues, voir le guide hormone de croissance prix France 2026.
Tésamoréline versus CJC-1295 : deux GHRH-analogues, deux philosophies
Deux peptides du même genre, deux mécaniques pharmacologiques différentes. Voilà comment les distinguer pour un protocole de recherche.
| Critère | Tésamoréline | CJC-1295 with DAC |
|---|---|---|
| Séquence | 44 AA, modif trans-3-hexenoique | 29 AA modif + bras DAC maléimide |
| Stabilisation | Résistance DPP-IV | Liaison covalente albumine |
| Demi-vie | 26-60 minutes | 5,8 à 8,1 jours |
| Profil GH | Pulsatile préservé | Continu sur 6+ jours |
| AMM clinique | FDA Egrifta 2010, EGRIFTA WR 2025 | Aucune |
| Données peer-reviewed | 412 patients NEJM + NAFLD Lancet HIV | 21 patients Teichman 2006 phase 1 |
| Préservation pulsatilité | Oui (administration brève) | Partielle (Sackmann-Sala 2007) |
Pour quoi choisir quoi ? Pour une étude qui veut préserver la pulsatilité naturelle de la GH tout en stabilisant le peptide, la tésamoréline a l’avantage : son profil DPP-IV-resistant donne une fenêtre d’activité de 60 minutes qui correspond à un pulse GHRH naturel élargi. Pour une étude qui vise une élévation IGF-1 chronique sur plusieurs jours, le CJC-1295 with DAC est mécaniquement plus pertinent. Et pour comparer les deux comme contrôle interne d’un protocole, on les utilise en bras parallèles avec les mêmes paliers µg/kg.
Pour aller plus loin sur le CJC-1295, voir le guide CJC-1295 dosage et pharmacocinétique.
Sources scientifiques et réglementaires
- Falutz J, Allas S, Blot K, et al. Metabolic effects of a growth hormone-releasing factor in patients with HIV. NEJM 2007;357:2359-2370. DOI
- Stanley TL, Fourman LT, Feldpausch MN, et al. Effects of tesamorelin on non-alcoholic fatty liver disease in HIV: a randomised, double-blind, multicentre trial. Lancet HIV 2019;6(12):e821-e830. PubMed 31611038
- Stanley TL, Feldpausch MN, Oh J, et al. Effect of tesamorelin on visceral fat and liver fat in HIV-infected patients with abdominal fat accumulation: a randomized clinical trial. JAMA 2014;312(4):380-389. PMC4363137
- Fourman LT, Stanley TL, Billingsley JM, et al. Effects of tesamorelin on hepatic transcriptomic signatures in HIV-associated NAFLD. JCI Insight 2020;5(15):e140134. JCI Insight
- Theratechnologies / FDA. EGRIFTA WR (tesamorelin F8) approval supplemental BLA, March 25, 2025. Theratechnologies press release
- FDA EGRIFTA WR prescribing information 2025. accessdata FDA label 022505s020
- Ellis RJ, Heaton RK, Tang B, et al. Effects of tesamorelin on neurocognitive impairment in persons with HIV and abdominal obesity. AIDS 2025. PubMed 39813152
- Baker LD, Barsness SM, Borson S, et al. Effects of growth hormone-releasing hormone on cognitive function in adults with mild cognitive impairment and healthy older adults. Arch Neurol 2012;69(11):1420-1429. PubMed 22869065
- Falutz J, Mamputu JC, Potvin D, et al. Body composition, hepatic fat, metabolic, and safety outcomes of tesamorelin: meta-analysis of RCTs. Diabetes Metab Syndr 2024-2026. ScienceDirect
- Falutz J, Mamputu JC, Potvin D, et al. Effect of tesamorelin in people with HIV with and without dorsocervical fat. Front Endocrinol 2023. PMC9947601
FAQ
Quelle est la différence entre Egrifta®, Egrifta SV® et EGRIFTA WR™ ?
Trois formulations successives de la même molécule (tésamoréline). Egrifta F1 (2010, formulation originale, reconstitution quotidienne, volume injectable plus important). Egrifta SV F4 (2019, concentration 4× supérieure, volume divisé par 4 mais reconstitution quotidienne). EGRIFTA WR F8 (mars 2025, concentration 8× supérieure à F1 et 2× à F4, reconstitution hebdomadaire). Toutes les trois sont bioequivalentes pharmacocinétiquement. La tésamoréline vendue en recherche RUO chez French Peptides ne correspond à aucune de ces trois formulations cliniques : c’est un lyophilisat brut destiné à des protocoles in vitro.
Pourquoi la tésamoréline cible-t-elle la graisse viscérale et pas la graisse sous-cutanée ?
L’axe GH/IGF-1 a une action lipolytique préférentielle sur le tissu adipeux viscéral via plusieurs mécanismes : densité plus élevée des récepteurs GH sur les adipocytes viscéraux, métabolisme hépatique de l’IGF-1 qui module la lipogenèse de novo, et effets indirects sur la lipolyse via les hormones contre-régulatrices. Les essais Falutz 2007 et Stanley 2019 ont confirmé empiriquement cette spécificité : la VAT diminue significativement, la SAT (sous-cutanée) reste stable. Ce qui en fait un outil intéressant pour étudier la pharmacologie sélective du compartiment graisse viscéral.
Stanley 2019 sur la NAFLD, c’est applicable hors VIH ?
Pas directement. L’essai Stanley 2019 a recruté exclusivement des patients VIH+ avec NAFLD documentée par ¹H-MRS. La cohorte HIV présente un microenvironnement métabolique particulier (antirétroviraux, inflammation chronique de bas grade) qui peut modifier la réponse pharmacologique. L’extrapolation à la NAFLD de la population générale reste à valider par des essais dédiés. Cela dit, la signature transcriptomique hépatique observée par Fourman et al. 2020 (réduction de la lipogenèse de novo via DNL pathway) est plausible hors-VIH, et plusieurs essais sont attendus.
Tésamoréline en France 2026 : disponibilité hospitalière ?
Egrifta® n’a pas d’AMM centralisée européenne. La disponibilité passe par procédures nationales. En France, la tésamoréline n’est pas commercialisée en officine de ville : la prescription est réservée aux services hospitaliers, en ATU/recommandation temporaire d’utilisation pour des cas spécifiques de lipodystrophie HIV documentée. Hors AMM française, elle n’est pas remboursée. Le composé tésamoréline vendu en recherche RUO chez French Peptides n’a aucun lien avec ce circuit hospitalier : c’est un lyophilisat de laboratoire destiné aux protocoles in vitro.
Pourquoi le combo Tésamoréline + Ipamorelin existe-t-il ?
Même logique que CJC-1295 + Ipamorelin : combiner un GHRH-analogue (Tésamoréline, voie GHRH-R / Gαs / cAMP) avec un GHS-R1a-agoniste sélectif (Ipamorelin, voie ghréline / Gαq / Ca²⁺). Les deux mécanismes activent la libération de GH par voies parallèles non-redondantes, donc l’AUC GH combinée est supérieure à la somme des effets individuels. Le combo Tésamoréline+Ipamorelin pré-formulé chez French Peptides simplifie la reconstitution pour les protocoles qui veulent étudier la stimulation maximale de l’axe GH avec une demi-vie GHRH-analogue plus courte que CJC-1295 with DAC.
Effets secondaires rapportés dans les essais cliniques ?
Falutz 2007 et Stanley 2019 rapportent un profil de tolérance globalement bon. Les événements indésirables les plus fréquents sont des réactions au site d’injection (érythème, douleur locale), une hyperglycémie modérée à surveiller (la GH stimule la néoglucogenèse), et occasionnellement œdèmes périphériques. Plus rarement : arthralgies, paresthésies. Pas de signal de toxicité chronique grave sur les 52 semaines des études d’extension. Le profil de tolérance EGRIFTA WR F8 mars 2025 est superposable à celui de la formulation F1.
L’unique GHRH-analogue avec validation clinique humaine
La tésamoréline est, en 2026, le seul GHRH-analogue à avoir réussi le parcours AMM. Falutz 2007 a posé la pharmacologie clinique du visceral fat, Stanley 2019 a étendu la portée à la NAFLD avec un signal robuste à -37 % de graisse hépatique, EGRIFTA WR mars 2025 a modernisé la formulation pour une reconstitution hebdomadaire pratique. Sur le front cognitif, les résultats sont plus nuancés : le bénéfice à 6 mois en cohorte HIV+ n’a pas été démontré significativement.
Pour la recherche en laboratoire, la tésamoréline reste un composé de référence. Sa pharmacocinétique connue, sa cascade Gαs/cAMP préservée, et son profil de tolérance documenté en font l’étalon-or des protocoles GHRH-analogues. À condition que la pureté HPLC soit garantie ≥99 % et que la traçabilité Made in Europe soit documentée.
Sourcer de la tésamoréline et combos en France
Tésamoréline 5 ou 10 mg, combo pré-formulé Tésamoréline + Ipamorelin. Pureté HPLC garantie ≥99 %, CoA disponible sur demande, lyophilisat sourcé Europe, expédié le jour même.