PANORAMA CLINIQUE 2026 · MÉDICAMENTS AMM ET CANDIDATS RECHERCHE
Médicaments contre l’obésité en France 2026 : panorama des AMM et candidats émergents en recherche
2026 marque une année charnière pour la pharmacothérapie de l’obésité. Wegovy attend toujours son remboursement en France, Mounjaro vient d’obtenir l’avis favorable de la HAS, et le pipeline phase 3 livre des résultats spectaculaires : retatrutide à -28,7 % en TRIUMPH-4, CagriSema à -20,4 % en REDEFINE-1, orforglipron à -12,4 % en oral. On a relu STEP-1, SURMOUNT-1, TRIUMPH-4, REDEFINE-1, SYNCHRONIZE-1 et ATTAIN-1 pour structurer ici un panorama clinique précis et un état des candidats peptidiques en recherche préclinique correspondants.

Quels médicaments contre l’obésité sont autorisés en France en 2026 ?
Quatre molécules avec AMM sont effectivement disponibles dans les pharmacies françaises au premier semestre 2026, avec des statuts de remboursement très différents. Le tableau suivant synthétise l’état des lieux à date.
| Médicament | Mécanisme | Efficacité publiée | Statut France 2026 |
|---|---|---|---|
| Wegovy (sémaglutide 2,4 mg) | Agoniste GLP-1 | -14,9 % à 68 sem (STEP-1) | AMM obésité, avis HAS favorable, remboursement en attente CEPS |
| Mounjaro (tirzépatide) | Double agoniste GLP-1/GIP | -20,9 % à 72 sem (SURMOUNT-1) | AMM diabète + extension obésité, remboursement S2 2026 attendu |
| Saxenda (liraglutide 3 mg) | Agoniste GLP-1 | -8,0 % à 56 sem (SCALE) | Partiellement remboursé depuis 2024 |
| Xenical / Alli (orlistat) | Inhibiteur lipase pancréatique | -2,5 à -3,5 kg vs placebo | AMM ancienne, sans ordonnance pour Alli (60 mg) |
Mysimba (naltrexone + bupropion) n’est plus distribué en France en 2026. Ozempic (sémaglutide 1 mg) reste indiqué uniquement dans le diabète de type 2 ; son détournement pour la perte de poids hors AMM a fait l’objet d’alertes ANSM en 2023 et 2024.
Wegovy (sémaglutide 2,4 mg) : la référence STEP-1
Wegovy est le sémaglutide à dose obésité (2,4 mg hebdomadaire). Le sémaglutide 1 mg, lui, est commercialisé sous le nom Ozempic pour le diabète de type 2. Même molécule, dosage différent, AMM différente. La distinction est administrative mais pharmacologiquement la voie d’action est identique : agonisme du récepteur GLP-1, qui ralentit la vidange gastrique, augmente la satiété centrale et améliore le contrôle glycémique.
L’essai pivot STEP-1 publié par Wilding et collaborateurs dans le NEJM en 2021 a inclus 1 961 adultes en obésité ou surpoids sans diabète, randomisés en sémaglutide 2,4 mg ou placebo pendant 68 semaines. Résultat principal : perte de poids moyenne de -14,9 % dans le bras sémaglutide contre -2,4 % sous placebo. Plus de 86 % des participants ont perdu au moins 5 % de leur poids initial.
Tarifs France 2026. Hors remboursement, le coût mensuel observé se situe entre 180 € et 260 € pour les doses intermédiaires, et grimpe jusqu’à 270-370 € pour la dose de maintenance 2,4 mg. La HAS a rendu un avis favorable au remboursement en décembre 2024 (SMR important, ASMR V), mais les négociations de prix avec le CEPS sont toujours en cours au S1 2026.
Profil de tolérance. Effets gastro-intestinaux fréquents et dose-dépendants : nausées (44 %), diarrhée (30 %), vomissements (25 %), constipation (24 %). Contre-indications absolues : antécédents personnels ou familiaux de carcinome médullaire de la thyroïde, syndrome NEM 2. Surveillance à instaurer chez les personnes à risque de pancréatite.
Mounjaro (tirzépatide) : double agoniste GLP-1/GIP, SURMOUNT-1
Le tirzépatide est le premier double agoniste GLP-1 / GIP commercialisé. La combinaison des deux voies d’incrétines apporte un effet additionnel : amélioration de la sensibilité à l’insuline et de la dépense énergétique via le récepteur GIP, en complément de l’effet satiété du récepteur GLP-1.
L’essai SURMOUNT-1 publié par Jastreboff et collaborateurs dans le NEJM en 2022 a randomisé 2 539 adultes en obésité ou surpoids sans diabète. À 72 semaines, la perte de poids moyenne a été de -15,0 % à 5 mg, -19,5 % à 10 mg, et -20,9 % à 15 mg, contre -3,1 % sous placebo. C’est le médicament anti-obésité le plus efficace actuellement en pharmacie française.
Statut France 2026. Mounjaro a obtenu l’AMM européenne pour l’obésité en plus de son indication initiale en diabète de type 2. La HAS a rendu un avis favorable au remboursement en décembre 2025. Le remboursement effectif est attendu au 2e semestre 2026 sous conditions strictes : IMC supérieur ou égal à 35 kg/m², échec d’au moins 6 mois de prise en charge nutritionnelle, prescription par un endocrinologue ou nutritionniste.
Tarifs. 230 à 440 €/mois selon le palier (2,5 à 15 mg) hors remboursement. Le profil de tolérance est globalement comparable au sémaglutide pour les effets gastro-intestinaux. Le double agonisme GLP-1/GIP n’augmente pas significativement les effets indésirables comparé au GLP-1 seul dans les essais publiés.
Saxenda et orlistat : les options anciennes encore disponibles
Saxenda (liraglutide 3 mg quotidien) est le premier agoniste GLP-1 dédié à l’obésité, mis sur le marché français en 2015. L’essai SCALE Obesity and Prediabetes publié par Pi-Sunyer et collaborateurs dans le NEJM en 2015 a documenté une perte de poids de -8,0 % à 56 semaines contre -2,6 % sous placebo. Saxenda est partiellement remboursé en France depuis 2024 sous conditions de prescription spécifiques. Le format quotidien injectable (vs hebdomadaire pour Wegovy et Mounjaro) reste un facteur de moindre observance.
Orlistat (Xenical 120 mg sur prescription, Alli 60 mg sans prescription) reste sur le marché français comme option ancienne, mécanisme totalement différent : inhibition de la lipase pancréatique, qui réduit l’absorption d’environ 30 % des graisses alimentaires. L’efficacité publiée est de -2,5 à -3,5 kg supplémentaires vs placebo (méta-analyse Torgerson 2004, Diabetes Care). Tolérance médiocre (stéatorrhée, urgences fécales, fuites) qui limite l’observance dans la pratique.
Calendrier réglementaire et remboursement en France 2026
Le parcours d’un médicament anti-obésité jusqu’au remboursement en France suit quatre étapes après l’AMM européenne (octroyée par l’EMA).
- Avis HAS sur le SMR et l’ASMR. La Commission de la Transparence évalue le service médical rendu (SMR) et l’amélioration du service médical rendu (ASMR). Pour Wegovy : SMR important, ASMR V (pas d’amélioration vs alternatives). Pour Mounjaro : avis similaire en décembre 2025.
- Négociations de prix avec le CEPS. Le Comité économique des produits de santé négocie le prix avec le laboratoire. C’est l’étape qui bloque actuellement Wegovy depuis fin 2024. Les laboratoires demandent en général un alignement sur les prix européens, le CEPS pousse à la baisse.
- Inscription au Journal Officiel. Une fois l’accord trouvé, l’arrêté de remboursement est publié.
- Conditions de prescription. Le remboursement est conditionné à des critères stricts : IMC seuils, durée de prise en charge nutritionnelle préalable, type de prescripteur (généraliste, endocrinologue, nutritionniste).
Pour Mounjaro, les conditions attendues au 2e semestre 2026 sont : IMC supérieur ou égal à 35 kg/m² (ou supérieur ou égal à 30 avec comorbidité métabolique), échec documenté d’une prise en charge nutritionnelle de 6 mois minimum (perte de poids inférieure à 5 %), et prescription initiale par un médecin spécialiste (endocrinologue, nutritionniste, médecin de la nutrition).
L’enjeu budgétaire pour la Sécurité sociale est important. Une étude DREES estime que 17 % des adultes français sont en obésité (IMC supérieur ou égal à 30) en 2024. Si même 5 % d’entre eux remplissent les critères de remboursement Mounjaro à 230-440 €/mois, l’impact annuel se chiffre en milliards d’euros, ce qui explique le rythme prudent du CEPS.
Pipeline 2026-2027 : retatrutide, CagriSema, survodutide, orforglipron
Quatre candidats anti-obésité ont livré des résultats phase 3 spectaculaires entre 2024 et 2026. Trois sont injectables hebdomadaires, un est oral quotidien. Le tableau résume l’état des données.
| Candidat | Mécanisme | Efficacité phase 3 | Statut 2026 |
|---|---|---|---|
| Retatrutide (Lilly) | Triple agoniste GLP-1/GIP/glucagon | -28,7 % à 12 mg, 68 sem (TRIUMPH-4) | Dépôt NDA Q4 2026 attendu |
| CagriSema (cagrilintide + sémaglutide) (Novo Nordisk) | Co-administration agoniste amyline + GLP-1 | -20,4 % à 68 sem (REDEFINE-1, NEJM 2025) | Dépôts réglementaires en cours |
| Survodutide (Boehringer / Zealand) | Double agoniste GLP-1/glucagon | -16,6 % à 76 sem (SYNCHRONIZE-1) | Phase 3 en cours, lecture SYNCHRONIZE-2 attendue 2026 |
| Orforglipron (Lilly) | Agoniste GLP-1 oral, petite molécule non peptidique | -12,4 % à 72 sem (ATTAIN-1, NEJM 2025) | Dépôts réglementaires globaux 2026 |
Trois lectures importantes de ce panorama. Premièrement : le retatrutide pose une nouvelle barre. -28,7 % en TRIUMPH-4 (publication par Lilly fin 2025), c’est l’effet pondéral le plus fort jamais documenté en phase 3, équivalent à environ 32 kg de perte absolue chez le patient moyen de l’essai. Deuxièmement : le CagriSema confirme que la co-administration de deux mécanismes complémentaires (amyline + GLP-1) atteint des niveaux d’efficacité du même ordre que le tirzépatide en monothérapie. Troisièmement : l’orforglipron oral, bien que moins efficace en valeur absolue, ouvre la voie de la voie orale qui est un changement de paradigme pour l’observance et le coût de fabrication.
Peptides correspondants en recherche préclinique : retatrutide, sémaglutide, tirzépatide, cagrilintide, survodutide
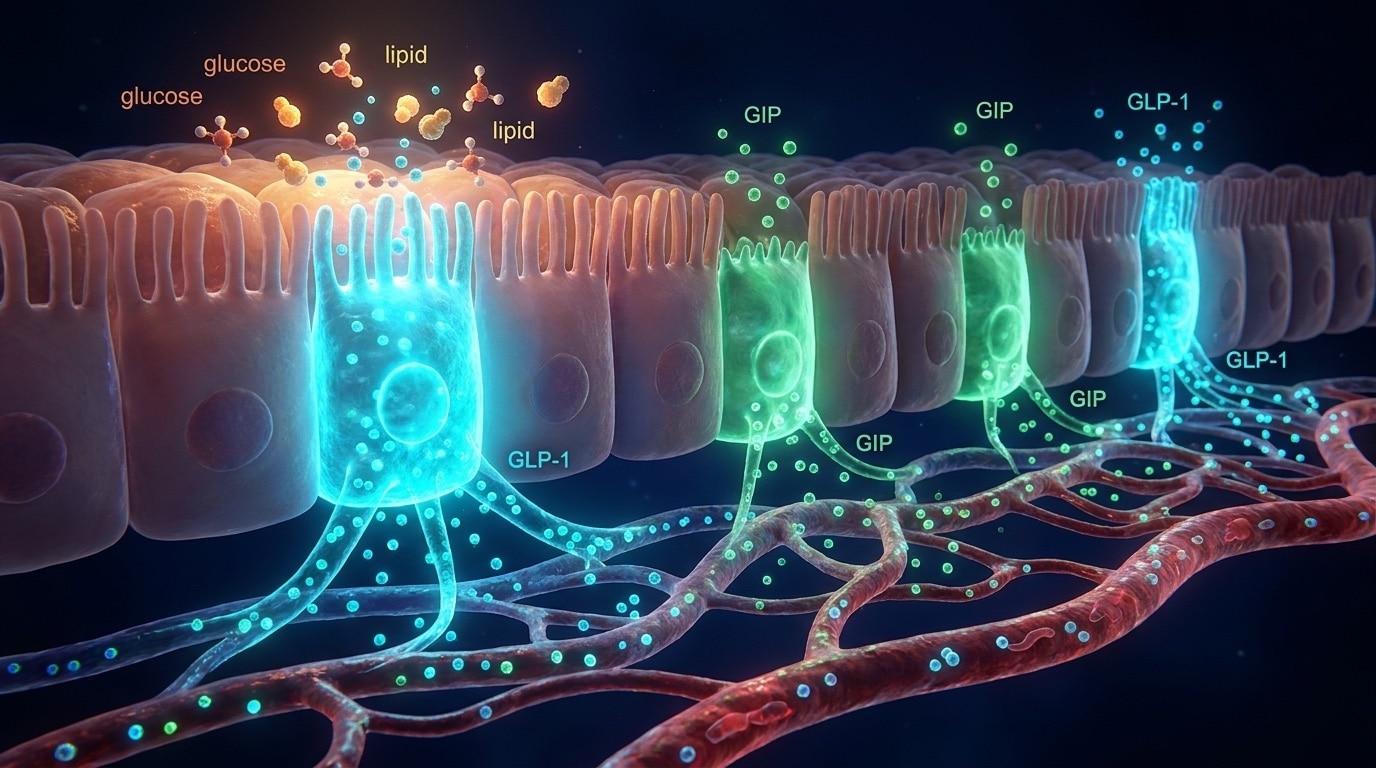
Pour le chercheur travaillant sur les voies des incrétines en modèle cellulaire, in vitro ou modèle animal, l’accès aux peptides au format de recherche lyophilisé est un outil méthodologique. Les molécules disponibles correspondent directement aux candidats cliniques décrits ci-dessus, mais leur usage est strictement laboratoire.
| Peptide de recherche | Cible moléculaire | Conditionnement laboratoire |
|---|---|---|
| Sémaglutide | Récepteur GLP-1 | Flacon lyophilisé 10 mg, pureté HPLC ≥99 % |
| Tirzépatide | Récepteurs GLP-1 + GIP (double agoniste) | Flacon lyophilisé 15 mg, pureté HPLC ≥99 % |
| Retatrutide | Récepteurs GLP-1 + GIP + glucagon (triple agoniste) | Flacon lyophilisé 10 mg, pureté HPLC ≥99 % |
| Cagrilintide | Récepteurs amyline et calcitonine | Flacon lyophilisé, pureté HPLC ≥99 % |
| Survodutide | Récepteurs GLP-1 + glucagon (double agoniste) | Flacon lyophilisé, pureté HPLC ≥99 % |
Pour la reconstitution au laboratoire, les peptides lyophilisés se remettent en solution dans de l’eau bactériostatique stérile à la concentration finale visée par le protocole. Voir le guide reconstitution + tableau de dosages pour la procédure standard. Pour le détail des prix et l’analyse coût-protocole sur le retatrutide, voir le guide prix retatrutide France 2026.
Profil de tolérance commun aux GLP-1 et candidats apparentés
Le profil d’effets indésirables est globalement homogène à travers la classe. Trois catégories méritent d’être rappelées.
Effets gastro-intestinaux fréquents et dose-dépendants. Nausées (35 à 50 % selon la molécule au palier maximal), diarrhée (20 à 35 %), vomissements (15 à 25 %), constipation (15 à 25 %). Ces effets sont concentrés sur la phase d’escalade de dose et s’améliorent en plusieurs semaines pour la majorité des patients dans les essais.
Contre-indications absolues. Antécédents personnels ou familiaux de carcinome médullaire de la thyroïde (CMT). Syndrome de néoplasie endocrinienne multiple de type 2 (NEM 2). Hypersensibilité connue à la molécule. Pour le retatrutide en phase 3, une mention spécifique doit être faite : la dysesthésie (sensations de picotements ou brûlure cutanée) a été rapportée chez 8,8 % au palier 9 mg et 20,9 % au palier 12 mg, contre 0,7 % sous placebo. C’est un effet propre à la composante glucagon, qui n’apparaît ni avec le tirzépatide ni avec le sémaglutide.
Précautions d’emploi. Surveillance clinique chez les personnes à antécédent de pancréatite aiguë. Surveillance ophtalmologique chez les diabétiques avec rétinopathie connue (cas rapportés d’aggravation initiale dans certains essais GLP-1). Adaptation de la prise alimentaire pour limiter les effets digestifs.
Sources scientifiques peer-reviewed et agences réglementaires
- Pi-Sunyer X. et al. A randomized, controlled trial of 3.0 mg of liraglutide in weight management. SCALE Obesity and Prediabetes. New England Journal of Medicine, 2015.
- Wilding J.P.H. et al. Once-Weekly Semaglutide in Adults with Overweight or Obesity. STEP-1 trial. New England Journal of Medicine, 2021.
- Jastreboff A.M. et al. Tirzepatide Once Weekly for the Treatment of Obesity. SURMOUNT-1. New England Journal of Medicine, 2022.
- Jastreboff A.M. et al. Triple-Hormone-Receptor Agonist Retatrutide for Obesity (Phase 2 trial). New England Journal of Medicine, 2023.
- Eli Lilly. TRIUMPH-4 Phase 3 results: retatrutide 28.7% weight loss in obesity and knee osteoarthritis. Investor announcement, 2025. Lilly investor
- REDEFINE-1 study group. Cagrilintide-Semaglutide in Adults with Overweight or Obesity. New England Journal of Medicine, 2025. NEJM
- Boehringer Ingelheim. SYNCHRONIZE-1 Phase 3 trial: survodutide 16.6% weight loss in obesity. Topline results announcement, 2025.
- ATTAIN-1 study group. Orforglipron, an Oral Small-Molecule GLP-1 Receptor Agonist for Obesity Treatment. New England Journal of Medicine, 2025. NEJM ATTAIN-1
- Torgerson J.S. et al. XENical in the prevention of diabetes in obese subjects (XENDOS) study. Diabetes Care, 2004.
- Haute Autorité de Santé (HAS). Avis de la Commission de la Transparence sur Wegovy et Mounjaro. 2024-2025.
- Agence Nationale de Sécurité du Médicament (ANSM). Mises en garde sur l’utilisation hors AMM des GLP-1 (Ozempic, Saxenda) à visée d’amaigrissement. Communications 2023-2024.
- European Medicines Agency (EMA). European public assessment reports : Wegovy, Mounjaro, Saxenda, Xenical.
Questions fréquentes : médicaments anti-obésité 2026 et candidats recherche
Quels médicaments anti-obésité sont autorisés en France en 2026 ?
Quel médicament anti-obésité est le plus efficace en 2026 ?
Wegovy et Mounjaro sont-ils remboursés en France en 2026 ?
Quelle différence entre Wegovy et Ozempic ?
Le retatrutide est-il disponible en France en 2026 ?
En résumé : où en est la pharmacothérapie de l’obésité en 2026
2026 est une année de bascule. Quatre médicaments avec AMM sont sur le marché français, dont Mounjaro qui devrait obtenir son remboursement effectif au S2 sous conditions strictes. Le pipeline livre des résultats sans précédent : retatrutide à -28,7 %, CagriSema à -20,4 %, survodutide à -16,6 %, orforglipron oral à -12,4 %. La barre d’efficacité monte de 5 points environ par an depuis 2021 (STEP-1 à -14,9 %, SURMOUNT-1 à -20,9 %, TRIUMPH-4 à -28,7 %).
Pour le chercheur travaillant sur les voies des incrétines en modèle cellulaire ou animal, l’accès aux peptides correspondants au format lyophilisé permet de mener des protocoles méthodologiquement comparables à ceux des publications de référence. Le sémaglutide, le tirzépatide, le retatrutide, le cagrilintide et le survodutide sont disponibles à pureté HPLC supérieure ou égale à 99 % avec CoA disponible sur demande, dans un cadre exclusivement de recherche in vitro.
Pour aller plus loin, voir notre guide prix retatrutide France 2026 et le guide complet des peptides en France 2026.
FRENCH PEPTIDES · INCRÉTINES RECHERCHE
Sémaglutide, tirzépatide, retatrutide, cagrilintide, survodutide grade laboratoire
Pureté HPLC garantie supérieure ou égale à 99 %, confirmation LC-MS, Made in Europe, expédié le jour même. Conditionnement lyophilisé, CoA disponible sur demande. Pour la recherche in vitro de laboratoire exclusivement.